|
Modelos
Atômicos Os modelos
atômicos são os aspectos estruturais dos átomos que foram apresentados por
cientistas na tentativa de compreender melhor o átomo e a sua composição. Em 1808, o cientista inglês John Dalton propôs uma explicação para a
propriedade da matéria. Trata-se da primeira teoria atômica que dá as bases
para o modelo atômico conhecido atualmente. A constituição da matéria é motivo de estudos desde a antiguidade. Os
pensadores Leucipo (500 a.C.) e Demócrito (460
a.C.) formularam a ideia de haver um limite para a pequenez das partículas. Eles afirmavam que elas se tornariam tão pequenas que não poderiam ser
divididas. Chamou-se a essa partícula última de átomo. A palavra é derivada
dos radicais gregos que, juntos, significam o que não se pode dividir. O Modelo Atômico de Dalton
Modelo atômico
de Dalton O Modelo Atômico de Dalton, conhecido como o modelo bola de
bilhar, possui os seguintes princípios: 1. Todas as
substâncias são formadas de pequenas partículas chamadas átomos; 2. Os átomos de
diferentes elementos têm diferentes propriedades, mas todos os átomos do
mesmo elemento são exatamente iguais; 3. Os átomos não se
alteram quando formam componentes químicos; 4. Os átomos são
permanentes e indivisíveis, não podendo ser criados nem destruídos; 5. As reações
químicas correspondem a uma reorganização de átomos. Modelo Atômico de Thomson
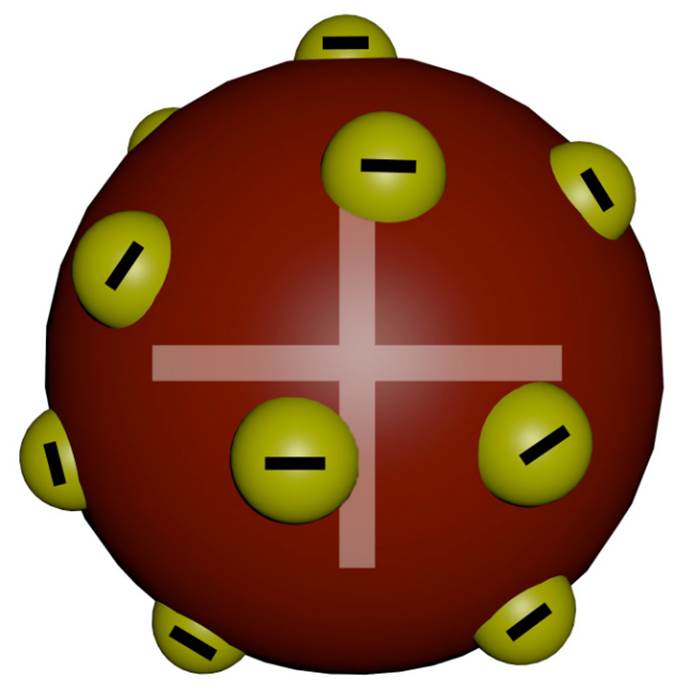
Modelo
Atômico de Thomson O Modelo Atômico de Thomson foi o primeiro a realizar a
divisibilidade do átomo. Ao pesquisar sobre raios catódicos, o físico inglês
propôs esse modelo que ficou conhecido como o modelo pudim de ameixa. Ele demonstrou que esses raios podiam ser interpretados como sendo um
feixe de partículas carregadas de energia elétrica negativa. Em 1887, Thomson sugeriu que os elétrons eram um constituinte
universal da matéria. Ele apresentou as primeiras ideias relativas à
estrutura interna dos átomos. Thomson indicava que os átomos deviam ser constituídos de cargas
elétricas positivas e negativas distribuídas uniformemente. Ele descobriu essa mínima partícula e assim estabeleceu a teoria da
natureza elétrica da matéria. Concluiu que os elétrons eram constituintes de
todos os tipos de matéria, pois observou que a relação carga/massa do elétron
era a mesma para qualquer gás empregado em suas experiências. Em 1897, Thomson tornou-se reconhecido como o “pai do elétron”. Modelo Atômico de Rutherford
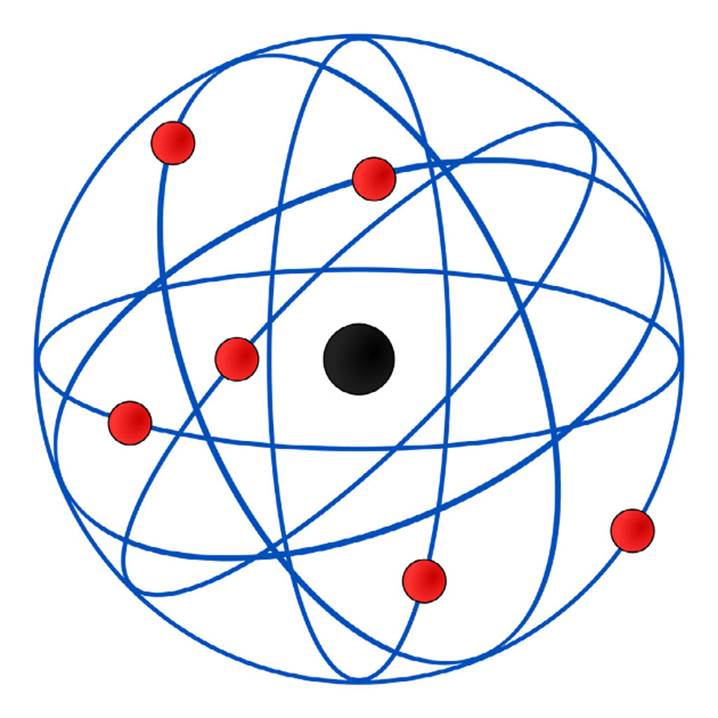
Modelo
atômico de Rutherford Em 1911, o físico neozelandês Rutherford colocou uma folha de ouro
bastante fina dentro de uma câmara metálica. Seu objetivo era analisar a
trajetória de partículas alfa a partir do obstáculo criado pela folha de
ouro. Nesse ensaio de
Rutherford, observou que algumas partículas ficavam totalmente bloqueadas e
outras partículas, que não eram afetadas, ultrapassavam a folha sofrendo desvios.
Segundo ele, esse comportamento podia ser explicados
graças às forças de repulsão elétrica entre essas partículas. Pelas observações, afirmou que o átomo era nucleado e sua parte
positiva se concentrava num volume extremamente pequeno, que seria o próprio
núcleo. O Modelo Atômico de Rutherford, conhecido como modelo planetário,
corresponde a um sistema planetário em miniatura, no qual os elétrons se
movem em órbitas circulares, ao redor do núcleo. Modelo de
Rutherford – Bohr
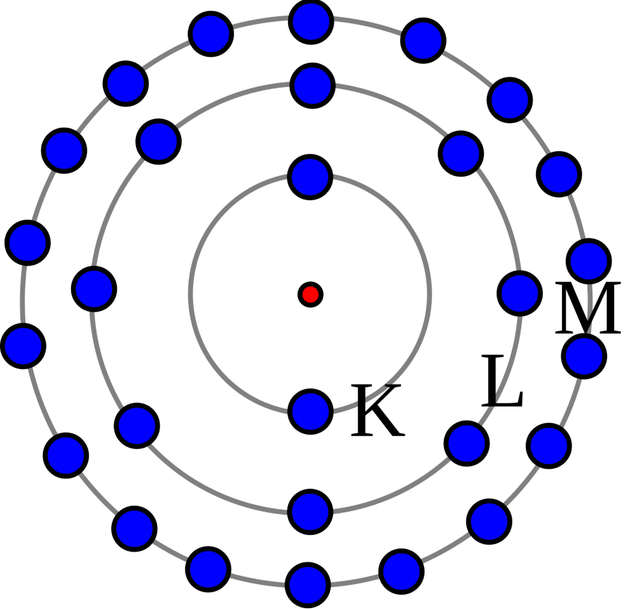
Modelo
Atômico de Rutherford-Bohr O modelo apresentado por Rutherford foi aperfeiçoado por Bohr. Por
esse motivo, o aspecto da estrutura atômica de Bohr também é chamado de Modelo
Atômico de Bohr ou Modelo Atômico de Rutherford-Bohr. A teoria do físico dinamarquês Niels Bohr estabeleceu as seguintes
concepções atômicas: 1. Os elétrons que
giram ao redor do núcleo não giram ao acaso, mas descrevem órbitas
determinadas. 2. O átomo é
incrivelmente pequeno, mesmo assim a maior parte do átomo é espaço vazio. O
diâmetro do núcleo atômico é cerca de cem mil vezes menor que o átomo todo.
Os elétrons giram tão depressa que parecem tomar todo o espaço. 3. Quando a
eletricidade passa através do átomo, o elétron pula para a órbita maior e
seguinte, voltando depois à sua órbita usual. 4. Quando os
elétrons saltam de uma órbita para a outra resulta luz. Bohr conseguiu prever
os comprimentos de onda a partir da constituição do átomo e do salto dos
elétrons de uma órbita para a outra. |